本文来自微信公众号:Nature Portfolio(ID:nature-portfolio),作者:Amber Dance,原文以The secret forces that squeeze and pull life into shape为标题发表在2021年1月13日《自然》的新闻特写版块上,头图来自:视觉中国
科学家正在研究机械力在人体中的作用——从胚胎到成年。
生命的最初,一个胚胎不分前后、头尾,就是一团简单的细胞。但很快,平滑的细胞团开始改变,液体聚集到细胞团中央,细胞像蜂蜜一样流动,占据它们在未来身体中的位置。细胞层像折纸一样折叠,构建出心脏、肠道和大脑。
如果没有挤压、弯曲和拉拽力使发育中的动物成形,这一切都不会发生。即使成年以后,其细胞也会继续对彼此之间以及来自环境的推力和拉力做出响应。
纽约洛克菲勒大学研究器官形成的发育生物学家Amy Shyer说,身体和组织的形成模式仍然是“我们这个时代最重要的、却知之甚少的问题之一”。几十年来,生物学家一直在集中研究基因和其他生物分子塑造身体的方式,这主要是因为这些信号的分析工具容易获得,而且一直在进步。相比之下,机械力受到的关注则少得多。
西班牙巴塞罗那加泰隆罗尼亚生物工程研究所的机械生物学家Xavier Trepat说,只研究基因和生物分子“就好比只用一半的字母表写一本书”。
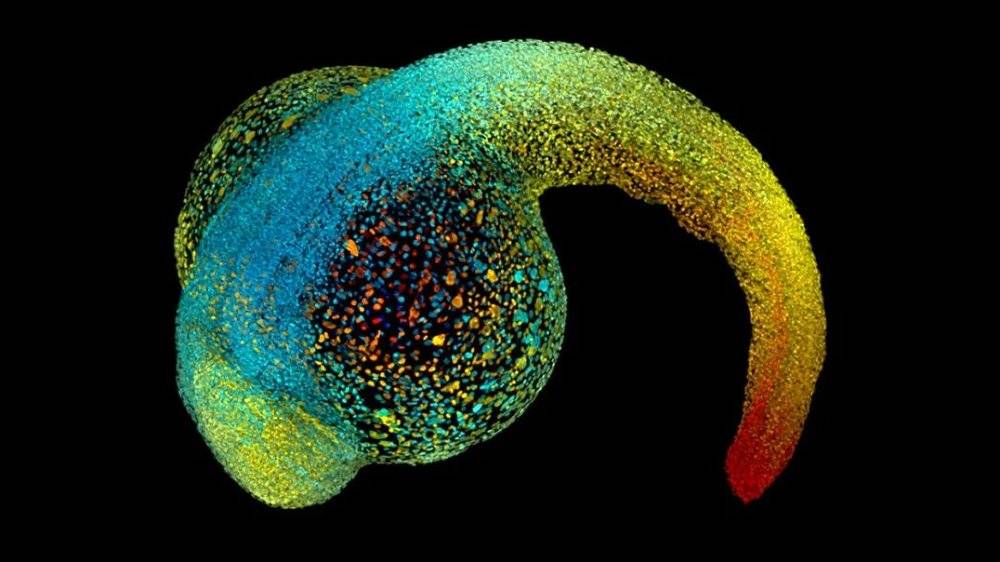
发育中的胚胎——如图中的斑马鱼——在成长过程中依靠物理作用力来塑造自己的形状。来源:Philipp Keller/ HHMI Janelia Research Campus
在过去的20年中,越来越多的科学家开始关注力学在器官和生物体各个发育阶段的重要性。研究人员开始定义细胞感觉、响应和产生力的机制。他们通过发明定制的工具和开发一些技巧,结合激光和微量移液器、磁性颗粒和定制的显微镜来实现。
大多数研究人员都在使用培养皿中培养的细胞或组织来探测力学信号,仅有少数几个小组在研究整个动物,这些动物中往往会发现与分离出的组织表现不同的机制。伦敦大学学院的发育生物学家Roberto Mayor表示,这些体内研究有许多挑战——例如要在复杂组织中测量微小的力——但它们对于理解力在雕刻生命中的作用至关重要。
少数意志坚定的科学家迎难而上,已经观察到了塑形生物的关键力量——从胚胎存在的初始阶段到疾病侵袭的生命晚期。将来,这些信息或能针对不孕症或癌症等问题设计出更好的干预措施。
“只要有形状的地方,就有力在发挥作用。”法国发育生物学研究所的发育生物学家Thomas Lecuit说。
从一开始就很有力
在胚胎成形之前,它必须打破平滑细胞团的对称性。在了解到基因和化学作用对这个过程的操控之后,科学家现在对力学有了更多的认识。巴黎居里研究所的生物学家Jean-Léon Maître说:“一点一点,机械力在发育过程中的作用逐渐显现出来。”例如,流体压力和细胞密度等物理特性是哺乳动物胚胎形成前、后、头、尾的关键。
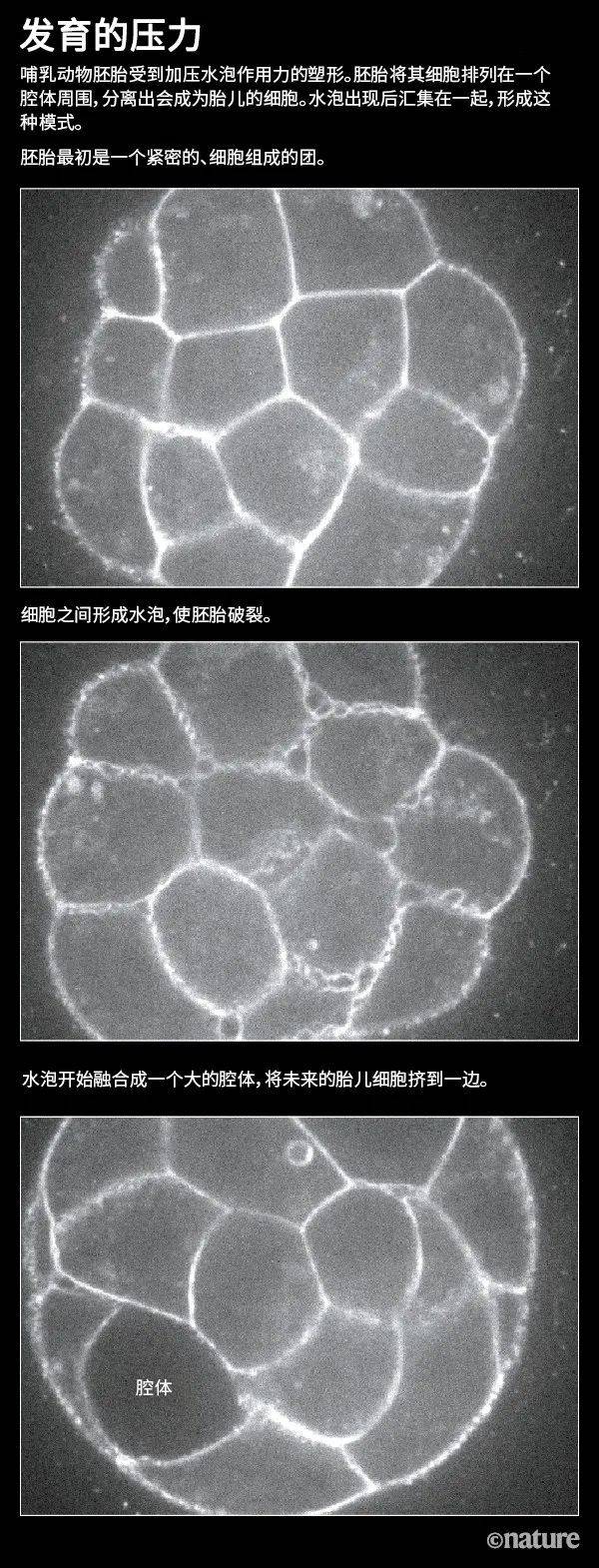
Maître团队研究了构成最早期小鼠胚胎的最初细胞团如何形成一个巨大的、充满流体的腔体。随着这个腔体的填满,即将形成胎儿的细胞被推向一边。这是第一个打破对称性的事件,它确保胚胎能正确植入子宫壁,也决定了胚胎的哪边是背部、哪边是腹部。但目前尚不清楚胚胎如何产生并定位腔体(见“发育的压力”)。
来源:参考文献2
当Maître团队对该过程进行细节成像时,他们发现了一些出乎意料的情况。“我们看到了这些小水泡,它们在细胞与细胞间形成。”Maître说,“它们转瞬即逝——如果成像速度不够快就会错过。”这些水泡中的流体来自胚胎周围的液体[1],这些液体由于外部水分子浓度较高而被迫进入内部。然后,团队看到了水从单个水泡流到一个大的腔体,Maître认为这可能是通过细胞之间的间隙。
研究人员通过观察跨细胞间隙的蛋白质证实了这种情况是如何发生的,这些蛋白质互相接触将细胞紧密地粘在一起[2]。水泡出现后,这些粘附蛋白似乎会随着细胞被推开而破裂。具有较少粘附蛋白的细胞更容易被分开。
Maître说,这是首次观察到加压流体可以通过破坏细胞之间的连接来塑形胚胎。为什么胚胎会通过强迫细胞分开的方式进行自我塑造?他说,“这种方式似乎效率低下,风险很大。” 他能想到的最好原因是,这个策略的演化形成不是因为它是最好的,而是因为它已经够好了。团队目前正在研究人类细胞,他希望对胚胎力学的进一步了解能帮助一些试管婴儿诊所确定哪些胚胎能实现成功受孕。
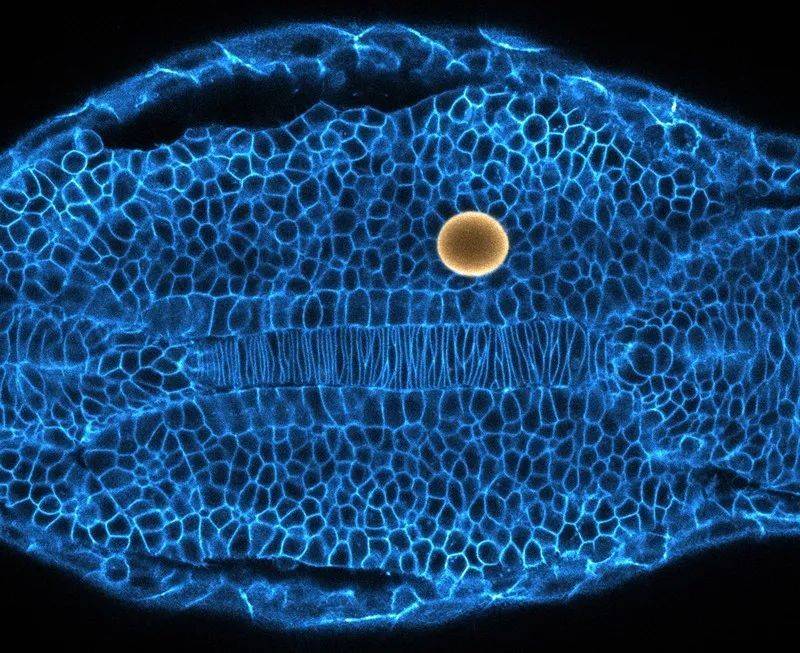
在后续发育中,胚胎又在一个方向上打破了对称性,分化出头和尾。加州大学圣塔芭芭拉分校的生物物理学家Otger Campàs追踪了斑马鱼(Danio rerio)胚胎中尾巴生长的过程[3]。他的课题组通过将负载了磁性纳米颗粒的油滴注射到细胞之间的间隔来测量其中涉及的力。然后该团队施加磁场使液滴变形,以便测量组织对推力如何响应。
为了对该斑马鱼胚胎的细胞进行推拉,研究人员用磁场使一个磁性液滴(黄色)变形。来源:Alessandro Mongera和Otger Campàs,加州大学圣塔芭芭拉分校
他们发现,尾巴在发育时的尖端处于被物理学家称为“流体”(fluid)的状态——细胞自由流动,受压时组织极易变形。离尾端越远的组织也越硬。Campàs回忆道,“我们当时知道它在变硬,但我们不明白其中的机制。”
细胞之间没有能够增加硬度的东西——没有能构成结构性基质的分子——但是当研究人员测量细胞之间的间距时,他们发现在湿软的尾尖中距离较大,越靠近头部距离越小[4]。当细胞聚集在一起时,组织也变硬了。Campàs将这种转变比作包装咖啡颗粒的过程:咖啡颗粒能自由地倒入袋中,但装得太紧,装满的袋子就像砖头一样硬。他打算研究这种机制是否是其他胚胎结构(如肢芽)形成的基础。
制造心脏和大脑
一旦发育中的胚胎做好了安排,各个器官就会开始形成。新加坡国立大学的发育生物学家Timothy Saunders说:“从根本上讲,我们对任何一个内脏器官的形成机制都不太了解。”(他指出,肠道是一个例外。)
情况已经有所改变。例如,Saunders的小组用果蝇Drosophila的胚胎研究心脏的形成。一个关键事件是,两块组织聚到一起形成一个管,这个管最终会成为心脏。每块组织含有两种心肌细胞。这些组织必须正确组合,就像拉拉链一样,镜像配对,才能得到健康的心脏。“我们经常看到组合发生错配随后被修正。”Saunders说,“是什么引起了这种修正?”
原来是来自心脏细胞自身的一种力量。名为肌球蛋白II的蛋白质是能使肌肉细胞收缩的蛋白质的近亲,已知其在拉拉链的过程中会从每个细胞的中心流向细胞的边缘。当时还是研究生的Shaobo Zhang——现正在准备加州大学旧金山分校的博士后职位——想知道肌球蛋白是否会产生这些配对细胞结合的反作用力,打破错配型之间的连接。
为了验证他的理论,Zhang用激光将成对的细胞切开。这些细胞迅速分离,就像一根拉紧的橡皮筋突然被剪断了一样。Saunders说:“我们可以看到漂亮的反冲。”但是,当团队切开缺乏肌球蛋白II的细胞时,“什么都没有发生”。肌球蛋白就像用手指拉橡皮筋的动作,从内部产生了连接的反作用力[5],让不匹配细胞之间的连接断开,进而有机会找到正确的配对。
英国剑桥大学的研究人员在非洲爪蟾Xenopus的胚胎中发现,简单的细胞增殖也能发出信号,指示细胞正确地自我排布。物理生物学家Kristian Franze领导的团队已经发现,随着眼脑连接逐渐形成,眼内神经元会让它们的轴突(轴突是神经元用于互相接触的长突触)沿着由脑组织不同硬度定义的路径延伸。在发育的大脑中,眼睛的轴突会跟随较软的组织向中枢延伸[6]。
为确定该路径何时以及如何形成,团队特制了一个显微镜。使用这个显微镜可以在观察在体过程的同时利用微小的探针测量组织的硬度[7]。在埃尔朗根-纽伦堡大学医学物理和微组织工程研究所担任负责人的Franze说,他们看到硬度梯度在轴突到达并沿其延伸的约15分钟前出现。
硬度梯度是如何出现的?和发育中的斑马鱼尾巴一样,青蛙大脑中较硬的组织似乎包含更高密度的细胞。当团队阻止发育胚胎中的细胞分裂时,硬度梯度就不再出现,轴突也找不到路径了。将空间塞满细胞似乎是引导神经系统连接的一种快速有效的方法。
持续的压力
发育成熟的动物在继续成长或应对疾病的过程中也必须与力抗衡。例如,当身体膨胀时,皮肤也会生长以覆盖它。外科医生在乳房重建术中利用了这一点,该手术需要更多的皮肤以覆盖植入物。首先,他们插入一个“气球”,并在几个月内注入盐水逐渐使之胀大,拉伸原有的皮肤,直至长出足够的新皮肤后再进行二次手术。
但是,皮肤细胞是如何响应这种压力并增殖的呢?干细胞生物学家Mariaceleste Aragona在比利时布鲁塞尔自由大学做博士后时,与Cédric Blanpain合作解决了这个问题。她在小鼠皮肤下植入了一种自膨胀水凝胶小球[8]。随着水凝胶吸收液体达到4毫升的终体积,皮肤也在其周围拉伸。在植入水凝胶的一天之内,Aragona看到皮肤外层下的干细胞开始增殖,提供了能分化成新皮肤的原材料。
但是并非所有的干细胞都能响应这种拉伸而增殖——只有一个之前未知的亚群会开始输出新的干细胞。“我们仍然不知道原因”,目前在哥本哈根大学工作的Aragona说。Blanpain补充道,阐明此系统有望破解促进皮肤生长的方法,用于外科手术重建或创伤愈合。
组织的力学特性在异常细胞生长(如癌症)中也起了作用。Trepat说:“实体肿瘤比正常组织硬。”他说,部分原因是由于细胞周围过量存在一种被称为细胞外基质的纤维网状物,也因为癌细胞本身正在增殖。
Trepat解释道,“硬度会增加癌细胞的恶性”,如果科学家能够理解其中原因,他们就有可能设计出改变这些物理特性并降低癌症危险性的疗法。
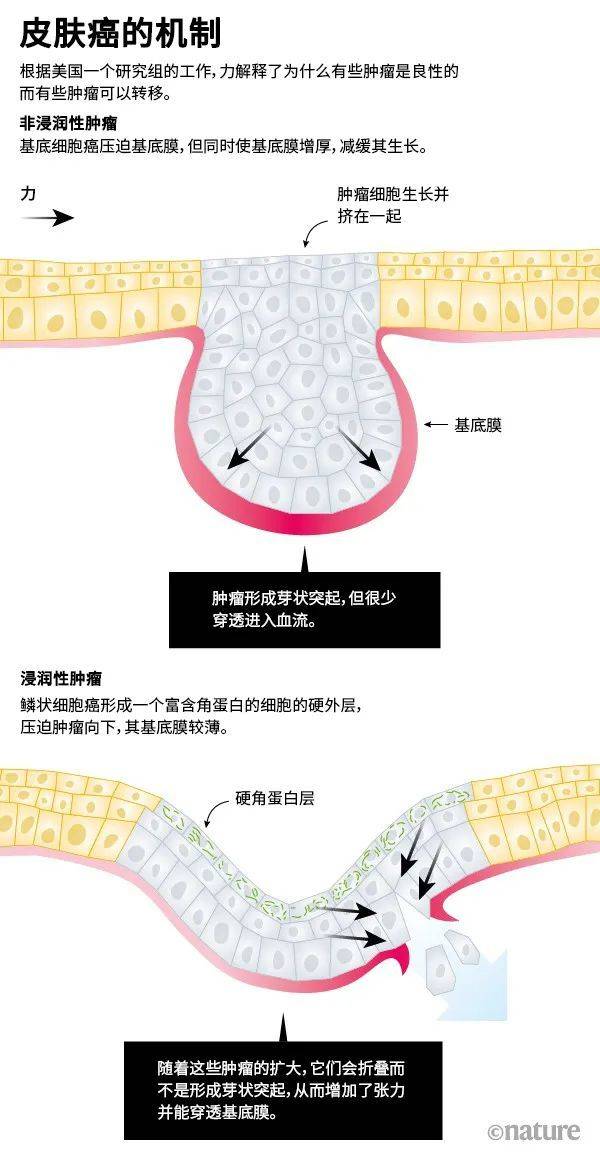
在一项相关研究中,洛克菲勒大学的研究人员已确认机械力可以解释为什么有些皮肤癌是良性的而有些是恶性的。皮肤干细胞会产生两类癌症:不会扩散到皮肤外的基底细胞癌和浸润性的鳞状细胞癌。这两种都会挤压下层的基底膜,基底膜是一层结构蛋白,能将皮肤的外层与更深的组织分隔开。良性的基底细胞肿瘤几乎不会穿过基底膜,但侵略性较强的鳞状细胞肿瘤经常逃脱,在脉管系统中游走,并定植在身体的其他部位(见“皮肤癌的机制”)。
来源:参考文献9
干细胞生物学家Elaine Fuchs和Vincent Fiore在研究小鼠皮肤时发现,良性癌症会形成一个更厚、更柔软的基底膜,向下挤压时包含着肿瘤细胞的基底膜就像戴着手套一样。而侵袭性肿瘤会形成一个更薄的基底膜。
来自上方的力量也有助于浸润性肿瘤的逃脱。鳞状细胞癌形成一层硬的分化的皮肤细胞,称为角化珠。通过挤压肿瘤顶部,角化珠帮助肿瘤冲破脆弱的基底膜,就像一拳打破了玻璃[9]。
Fuchs表示,在开展这项研究之前,研究人员曾认为这些具有固定特征的分化的皮肤细胞不会产生机械力。她说:“我认为这才是最大的惊喜。”
接下来,Fuchs和Fiore计划研究细胞是如何感知这些机械力的,以及它们如何将力转化为可能生成更多基底膜或是促分化的基因表达程序。
洛克菲勒大学的发育生物学家Alan Rodrigues说,力和基因的关系是个关键问题。这不仅是皮肤癌的问题。他说:“力学中的深层问题其实是力与分子有什么关系的问题。”
其他人也在研究这种关系。Lecuit说:“这不是一刀切:‘一切都是基因的作用’或是‘一切都是力的作用’,而是两者之间一场有趣的对话。”
参考文献:
1. Schliffka, M. F. et al. Preprint at bioRxiv https://doi.org/10.1101/2020.09.10.291997 (2020).
2. Dumortier, J. G. et al. Science 365, 465–468 (2019).
3. Serwane, F. et al. Nature Methods 14, 181–186 (2017).
4. Mongera, A. et al. Nature 561, 401–405 (2018).
5. Zhang, S., Teng, X., Toyama, Y. & Saunders, T. E. Curr. Biol. 30, 3364–3377 (2020).
6. Koser D. E. et al. Nature Neurosci. 19, 1592–1598 (2016).
7. Thompson, A. J. et al. eLife 8, e39356 (2019).
8. Aragona, M. et al. Nature 584, 268–273 (2020).
9. Fiore, V. F. et al. Nature 585, 433–439 (2020).
© nature, doi: 10.1038/d41586-021-00018-x
本文来自微信公众号:Nature Portfolio(ID:nature-portfolio),作者:Amber Dance,原文以The secret forces that squeeze and pull life into shape为标题发表在2021年1月13日《自然》的新闻特写版块上
原创文章,作者:奋斗,如若转载,请注明出处:https://blog.ytso.com/industrynews/177957.html